Würzburg大学和Marburg大学的一个研究团队首次成功地通过实验证明,细菌代谢产物可以增加特定免疫细胞的细胞毒性活性,从而对免疫治疗肿瘤的效率产生积极影响。这项新研究的发现最近通过一篇题为《微生物短链脂肪酸调节CD8 T细胞反应,改善癌症的免疫治疗》的文章发表在《自然通讯》杂志上。研究人员乐观地认为,可以通过控制肠道微生物群的细菌种类组成来控制其对癌症治疗成功的影响。
据估计,每个人的消化道中大约有100万亿个细菌细胞,它们有几千种。它们被认为与慢性炎症肠道疾病的发展有关,可引发糖尿病,导致肥胖症,甚至神经系统疾病如多发性硬化症和帕金森氏症都有它们有关,此外还包括抑郁症和孤独症。
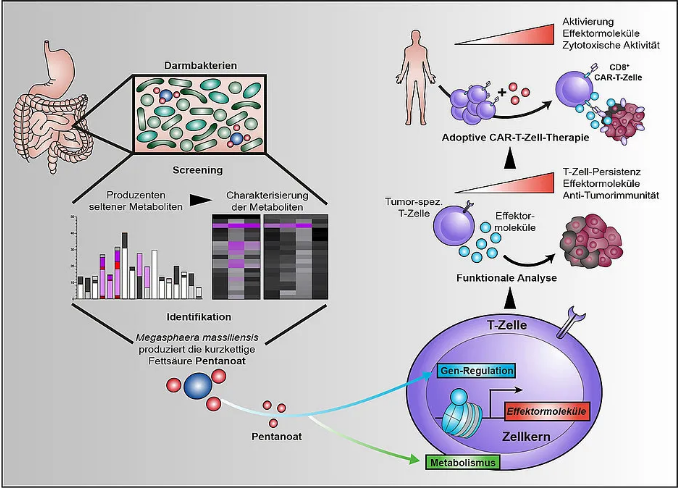
“我们能够证明短链脂肪酸丁酸,特别是戊酸可以增加CD8 T细胞的细胞毒性活性,”该研究的首席研究员Maik Luu博士说,他是Würzburg大学医院医学诊所和综合诊所II的博士后研究员。“CD8 T细胞有时也被称为杀伤细胞。作为免疫系统的一部分,它们的任务就是杀死那些对机体有害的细胞。”
20年来,微生物组一直是研究的焦点,高通量基因组测序技术的出现,使快速准确地分析这些细菌成为可能以来。有越来越多的发现表明,微生物组,也被称为人类第二基因组,不仅对消化具有核心的重要作用,还可以控制或者影响许多身体功能,特别是免疫系统。
短链脂肪酸作为肠道微生物群中最主要的一类代谢物。可诱发生物表观遗传的变化,一方面,其通过诱导能量代谢中枢调节因子,促进T细胞的代谢。另一方面,它们可以抑制特定的酶,这些酶通过调节遗传物质的可及性,从而抑制T细胞中的基因表达。
Luu博士指出:“当短链脂肪酸重新编码CD8 T细胞时,会增加促炎分子和细胞毒性分子的产生。”在实验中,戊酸脂肪酸的治疗提高了肿瘤特异性T细胞对抗实体肿瘤模型的能力。“当我们用CAR-T细胞治疗肿瘤细胞时,我们能够观察到同样的效果。”
正常的T细胞对肿瘤大多是无法特异识别的,但经过基因修饰的CAR-T细胞,可靶向识别肿瘤,实现精准治疗肿瘤。
Luu博士说:“这些数据表明,肠道细菌代谢物通过调节细胞代谢和基因调控,对肿瘤治疗产生了积极影响,尤其有利于CAR-T细胞在实体瘤方面的疗效”。
目前在这些病例中,使用转基因细胞治疗的效果远不如治疗血液病肿瘤(如白血病)有效。然而,科学家们认为,如果CAR-T细胞在应用于患者之前先用戊酸或其他短链脂肪酸治疗,这种情况可能会改变。
在这些新发现为肿瘤患者带来新的治疗方法之前,还有很长的路要走。下一步,研究团队将初步扩展所研究的肿瘤疾病的范围,除了实体肿瘤外,还将研究血液肿瘤疾病,如多发性骨髓瘤。此外,他们还将更深入地研究短链脂肪酸的功能,以确定靶向基因修饰的起点。

