近年来,全球掀起一股癌症免疫疗法新浪潮,使得该疗法逐渐成为癌症治疗的主流方式。巨噬细胞作为免疫反应的关键执行者,在癌症免疫治疗中发挥着重要的作用,并表现出广阔的发展前景。
本月,佐治亚州立大学的科研人员在Nature Communications/《自然-通讯杂志》发表了一篇题为Intratumoral SIRPα-deficient macrophages activate tumor antigen-specific cytotoxic T cells under radiotherapy(“瘤内调节蛋白α(Sirpα)在放射治疗下,可望激活体内T细胞中的特异抗原,从而治愈癌症)。这是一项开创性研究,它有望引导学术界开发一种基于巨噬细胞的新型免疫疗法,有效治疗多种晚期癌症。
从生理学看,巨噬细胞就像是人体的侦察兵,遇到潜在的威胁会吞噬摧毁它们。但由于癌细胞很狡猾,它经常会伪装成正常细胞,通过正常细胞所依赖的共同生理机制来逃脱巨噬细胞的免疫监视,以提升自身的分裂能力,从而抑制人体免疫反应。
肿瘤的这种逃逸能力的罪魁祸首,是一种名为“调节蛋白α(Sirpα)” 的受体,它是一种骨髓白细胞表达的抑制性调节剂,它主要是通过与自我识别标记 CD47相互作用来抑制吞噬细胞发挥作用,使得放射治疗 (RT) 诱导的杀瘤免疫受到严重限制。
SIRPα/CD47通路的深入研究
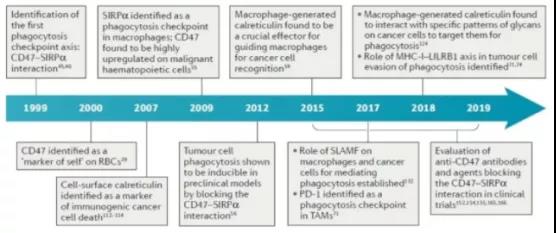
CD47-SIRPα信号通路又被称为“别吃我”信号,最早于1990年发现,但直到1999年科学家利用单克隆抗体等技术,才证实了SIRPα与CD47之间的交互作用。随即科学家们用二十年时间进行深入研究,最终如本月《自然》发表的论文,探究出一种基于Sirpα缺陷的巨噬细胞疗法来对抗癌症,来对抗癌症!
Sirpα缺陷的免疫疗法,抗癌疗效好副作用小
研究人员首先构建体内结肠癌模型(MC38)如下图,随后用基于Sirpα缺陷的巨噬细胞疗法来治疗癌症,验证该细胞疗法的治疗效果。
研究发现,局部放化疗治愈了患有晚期肿瘤的Sirpα缺陷小鼠的结直肠癌;而且接受治疗的患癌小鼠,并无明显不良反应;还表现出与健康小鼠相似的正常寿命(约18个月)。
研究团队认为:该研究说明通过Sirpα缺陷基因的治疗,巨噬细胞可通过引发炎症和激活肿瘤特异性T细胞,启动针对癌症的强大免疫反应,并可最大限度的降低对健康细胞的不利影响。
Sirpα缺陷的免疫疗法,无论新发或晚期癌症,疗效俱佳
为了确定经治疗后的Sirpα缺陷小鼠体内的长期抗肿瘤免疫是否已经生成,研究人员对已根除结肠癌的Sirpα 缺陷小鼠进行了肿瘤再移植试验,将MC38细胞(小鼠结肠癌细胞)重新接种到小鼠体内。令人惊喜的是,癌细胞并未在小鼠体内增殖扩散。说明这种基于巨噬细胞的新型免疫疗法,不仅可以短期治疗癌症,还可以让小鼠获得长期的抗肿瘤免疫能力。
与此同时,研究人员还发现,在给接种了MC38(小鼠结肠癌细胞)的小鼠,注射Sirpα缺陷小鼠的灭活肿瘤细胞血清后,亦可成功的抑制癌细胞的扩散。说明这种免疫疗法对新患肿瘤的小鼠,同样有效。Sirpα缺陷小鼠的血清,竟然也还具有防止新肿瘤形成的能力!
综上
这项研究表明:Sirpα 是肿瘤微环境免疫改变的主要操控者;针对Sirpα缺陷的免疫治疗,与放化疗相结合,或可成为一种“泛癌疗法”。或可成为指引人类对抗所有癌症的灯塔!
迄今为止,该治疗方法已经针对整个 NCI-60 癌症组合进行了测试,囊括了60 种不同的人类肿瘤细胞系,如白血病、黑色素瘤、肺癌、结肠癌、脑癌、卵巢癌、乳腺癌、前列腺癌和肾癌等,并且已经被发现有显着疗效。
鉴于该疗法的重要意义,美国国家癌症研究所、乔治亚研究联盟等机构均给予研究经费资助;美国食品和药物管理局(FDA)也批准该疗法开展进一步的新药研究,并计划于2022年进行人体临床试验。我们可以相信一种有望治疗多种晚期癌症的免疫治疗即将上市!

