免疫检查点抑制剂(ImmuneCheckpoint Inhibitors, ICI)的出现已经改变了多种肿瘤的治疗格局,为部分患者带来了前所未有的长生存。然而尽管ICI的优势在于持续的反应,部分患者使用ICI治疗无效,存在原发性耐药;也有部分初始反应的患者最终产生获得性耐药。
目前对ICI耐药的理解还很有限。之前总结过抗体类药物的耐药机制。PD-1/PD-L1抑制剂也属于单克隆抗体,但是和针对确切靶点的抗体作用机制不同,因而耐药机制也有所不同。现将PD-1/PD-L1抑制剂的作用机制和耐药机制进行总结。
作用机制
ICI通过活化免疫系统产生抗肿瘤免疫反应。T细胞是ICI疗法的关键,T细胞介导的免疫由PD-1/PD-L1免疫检查点通路进行控制,以调节T细胞的活化和效应功能,维持自身耐受。此外,PD-1/PD-L1通路也可控制其他固有和适应性免疫细胞,协同维持免疫效应。
除了造血干细胞和抗原提呈细胞外,肿瘤细胞可以表达PD-L1配体。当PD-L1结合T细胞等免疫效应细胞表面的PD-1时,可导致胞浆免疫受体磷酸化,招募SHP2,通过T细胞受体下游信号通路介导免疫抑制功能。结合T细胞后,PD-1导致ZAP70和CD3ξ去磷酸化,干扰炎性反应。SHP2也可以抑制RAS/MEK/ERK通路,控制细胞增殖,生长和生存。
ICIs则可以通过结合PD-1或PD-L1而抑制PD-1/PD-L1通路活化,再活化细胞毒T细胞及其他免疫细胞,共同起到杀伤肿瘤细胞的作用。
耐药机制
ICI的耐药可分为两大类:1. 原发性耐药,患者对ICI治疗完全无反应,用药后出现快速进展;2. 获得性耐药:患者初始对ICI反应,最终出现临床和/或影像学进展。
综合既往临床研究报道,不同类型肿瘤对ICI单药初始反应不同,反应率约为10%~70%。而获得性耐药发生率在不同肿瘤中也不同,例如接受纳武利尤单抗治疗的黑色素瘤患者中,39%的反应者在5年随访内进展,而一项汇总分析显示非小细胞肺癌(Non-Small-Cell Lung Cancer, NSCLC)患者接受纳武利尤单抗治疗过程中,65%的反应者在4年随访内进展。
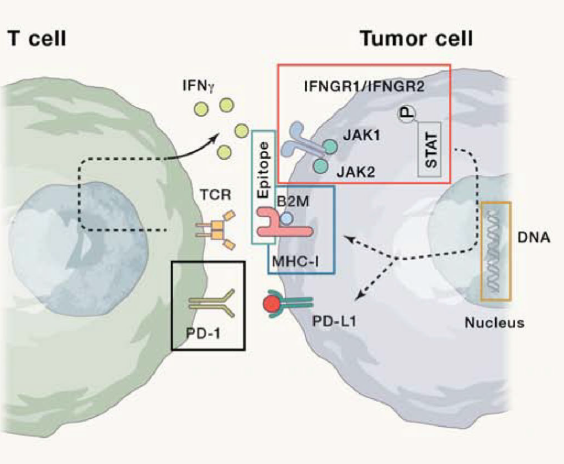
ICI的原发和获得性耐药机制有所区别而又存在重叠。现将主要耐药机制进行总结(图1)。
图1 常见耐药机制(来源DOI:10.1016/j.ccell.2020.03.017)
原发性耐药机制1.PD-L1表达。PD-L1表达对于ICI的反应十分重要。这不仅是由于药物需要靶向PD-1受体-配体的相互作用,也由于PD-L1表达和活化CD8+T细胞反应和抗原提呈等其他免疫活化行为相关。因此,PD-L1阴性或低表达患者更可能对ICI耐药。
2.肿瘤突变负荷(Tumor Mutational Burden, TMB)。TMB是由致癌原、基因组不稳定或错配修复缺陷而导致的突变增加。低突变负荷和低新抗原水平和反应不佳相关。
3.介导免疫的关键信号通路受损。例如干扰素-γ(Interferon-γ, IFN-γ)是重要的细胞因子,可以通过促进CD8+T细胞活性,抗肿瘤细胞增殖,促进凋亡和诱导Ⅰ类主要组织相容物(MajorHistocompatibility Complexe, MHC)上调启动和维持强力抗肿瘤反应。
效应T细胞释放的IFN-γ通过JAK/STAT通路激活肿瘤细胞级联信号通路而调节Ⅰ类MHC和PD-L1表达,诱导肿瘤细胞死亡。该途径的关键步骤是IFN-γ结合至异二聚体IFNGR1/IFNGR2而活化受体相关激酶JAK1和JAK2。临床研究显示JAK1或JAK2的功能丢失性突变以及IFNGR1/IFNGR2的突变可导致ICI原发性耐药。
4.微生物肠道菌群也可能是原发性免疫耐药的机制之一。肠道菌群和免疫系统的Th1,Th2,Th17和Treg等效应细胞活性相关。一项动物研究显示给予小鼠健康供体来源的11种肠道细菌株可以增强ICI抗肿瘤活性,通过诱导肠道IFN-γ而产生CD8+T细胞。
5.肿瘤表观遗传特征表观遗传机制包括DNA甲基化,组蛋白调节,核小体重塑,非编码RNA表达异常等。表观遗传异常可导致肿瘤相关基因异常表达,导致肿瘤发生和发展。由于表观遗传也可以导致免疫细胞功能改变,因此也和免疫治疗疗效相关。
表观遗传调节异常可引起免疫检查点表达异常,影响抗原提呈和T细胞至肿瘤微环境(TumorMicroenvironment, TME)的迁移,引起细胞因子释放和T细胞活化过程。主要的表观遗传机制是甲基化。DNA甲基化可以起到抑制性作用,阻止肿瘤抑制因子和凋亡基因表达。另外还有组蛋白乙酰化,此过程可导致基因表达增加,促进转录因子招募。
PD-1,PD-L1和CTLA-4的启动子DNA甲基化和蛋白表达呈反相关,导致PD-L1等标志物表达下调,并可干扰IFN-γ通路的正常功能。
6.克服原发性耐药克服原发性耐药的方法主要是联合治疗策略,例如ICI联合化疗或靶向药物可以提高反应率。寻找PD-L1表达,TMB,肿瘤浸润淋巴细胞(Tumor Infiltrating Lymphocytes, TILs)或相关基因表达等预测生物标志物有助于筛选获益人群。另外开发克服耐药的药物,如表观遗传药物联合免疫治疗也是目前积极研究的方向。
获得性耐药机制1.抗原提呈机制缺陷T细胞活化依赖于识别抗原提呈细胞上的MHC抗原。Ⅰ类MHC的肿瘤抗原提呈通过协同多种基因表达而介导,一个关键基因是β2-微球蛋白(Beta-2-Microglobulin, B2M),B2M可反映Ⅰ类MHC分子的稳定性和肽类装载。
免疫治疗后B2M功能丢失性突变可导致Ⅰ类MHC丢失,是肿瘤逃逸免疫消除作用的重要分子路径之一。目前在黑色素瘤、NSCLC等多种肿瘤免疫治疗进展时发现过B2M的获得性截短突变,杂合子丢失(Loss OfHeterozygosity, LOH)和移码突变。此外,Ⅰ类MHC和B2M蛋白表达水平下降可能也参与此耐药机制。
2.IFN-γ信号通路缺陷IFN-γ信号通路异常也可以导致获得性耐药。有研究使用获得性JAK2突变的患者细胞建立细胞系,或使用CRISPR-Cas9编辑JAK1或JAK2突变细胞系,可以确定JAK蛋白丢失和肿瘤细胞对IFN-γ敏感性丢失、Ⅰ类MHC丢失和PD-L1表达丢失相关。
3新抗原消除新抗原特异性T细胞是ICI反应的主要驱动。因此,编码肿瘤特异性新抗原的体突变丢失可通过克隆选择,表观遗传抑制,拷贝数丢失等机制导致免疫逃逸和临床进展。
对比患者免疫治疗前后的外显子测序数据,可以发现产生新抗原的众多突变。体外研究显示很多丢失的新抗原肽共同刺激可导致克隆性T细胞扩增,表明这些新抗原为免疫相关,可以驱动选择压力来消除敏感克隆,导致获得性耐药克隆的生长。
4.肿瘤介导免疫抑制/排斥和耐药基因表达临床前模型中,调节PI3K活性的肿瘤抑制基因PTEN丢失可增加免疫抑制细胞因子表达,降低T细胞效应因子IFN-γ,导致抑制性T细胞介导的浸润和免疫抑制[2]。
和PTEN丢失类似,WNT-β-catenin,mTOR,Kras等信号通路也和免疫抑制性细胞因子产生及免疫耐受相关。
还有研究发现耐药肿瘤表现出免疫抑制相关的转录特征,包括IL10,VEGFA和VEGFC等免疫抑制基因,AXL,ROR2,WNT5A, LOXL2,TWIST2,TAGLN和FAP等上皮间质转化转录因子,CCL2, CCL7,CCL8,CCL13等单核和巨噬细胞趋化因子,血管生成和MAPK通路抑制基因等。
5.其他抑制性检查点有研究报道获得性耐药时可出现其他T细胞检查点上调,包括TIM3,LAG3,VISTA等[2]。
6.肿瘤细胞的可变性和去分化状态在黑色素瘤等肿瘤的研究发现肿瘤细胞可以去分化,获得干细胞或祖细胞样特性而导致免疫识别的逃逸。
在鳞状细胞中,去分化肿瘤细胞可获得干细胞样特性,表达免疫调节分子CD80,导致免疫攻击逃逸。同样,去分化浸润细胞可通过PD-L1失调等逃逸免疫监视。单细胞分析显示肺癌细胞具有异质性分化状态,这些状态具有不同的具有不同免疫监视敏感性和转移性克隆能力。
7.TME的效应T细胞浸润免疫治疗反应高度依赖于改变TME中效应T细胞浸润,例如新抗原异常,T细胞活化异常甚至T细胞不能达到肿瘤都可以导致耐药。大量活化肿瘤特异性T细胞和效应T细胞在TME的浸润很关键。TGF-β诱导下,基质细胞在肿瘤细胞周围组成物理性肌纤维屏障,可阻止浸润和影响T细胞迁移,导致耐药发生。
8.T细胞耗竭共刺激和共抑制的平衡决定T细胞活化和扩增程度。共刺激可扩大T细胞活化,而抑制性受体,抑制性可溶性介导物,免疫抑制TME的部分细胞亚群和代谢因子可导致T细胞耗竭。
TME的免疫抑制信号可通过影响抑制性受体表达,改变代谢通路,调节表观遗传状态和改变转录因子特征而导致瘤内T细胞耗竭。
目前有很多关于增强T细胞免疫力的研究正在进行,包括肿瘤浸润细胞的适应性转化,内源性外周血来源T细胞,CAR-T,新抗原疫苗等疗法的研究在不断进行,以逆转T细胞功能不全状态。
9.机制不明尽管关于PD-1/PD-L抑制剂的耐药机制是当前免疫治疗的研究热点,而且也取得了很大进步,但是由于缺乏获得性耐药的确切定义,免疫治疗进展后再活检比靶向治疗少见,缺乏有效工具来综合发现肿瘤、宿主和/或TME的免疫耐受机制,目前大多数免疫耐药机制依旧不明。
10.克服获得性耐药目前还没有针对获得性耐药获批的治疗。明确具体耐药机制,研发新型药物是主要发展方向。针对IFN-γ,TIM3,LAG3,和减少T细胞耗竭的疗法已经进入临床研究阶段。
小结
综上,PD-1/PD-L抑制剂的耐药机制可总结为缺乏抗原、抗原处理或提呈异常,T细胞排斥或耗竭,信号通路异常,肿瘤细胞的结构性PD-L1表达降低,以及外在因素如微生物,宿主因素和基因易感性等。进行全基因组CRISPR-Cas9突变筛查是明确耐药机制的良好方法。积极发展新技术,进行耐药后临床研究,研发基于耐药机制的新型药物是克服ICI耐药的关键。

